Рады, что вам понравилась статья 😊
Лабораторная работа №7 Свойства белков Цветные реакции на белки и аминокислоты. С опытами: Биуретовая реакция, Реакция на «слабосвязанную серу»,Ксантопротеиновая реакция белков, Реакция Адамкевича (на присутствие в белках триптофана), Нингидриновая реакция, Реакция Сакагучи.

Значение цветных реакций состоит в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах и установить аминокислотный состав различных природных белков. Эти реакции применяются как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот. Некоторые реакции присущи не только белкам, но и другим веществам, например, фенол, подобно тирозину, дает розово-красное окрашивание с реактивом Миллона, поэтому проведения одной какой-либо реакции для установления наличия белка не достаточно.
Существует два типа цветных реакций: 1) универсальные – биуретовая (на все белки) и нингидриновая (на все а-аминокислоты и белки); 2) специфические – только на определенные аминокислоты как в молекуле белка, так и в растворах отдельных аминокислот, например реакция Фоля (на аминокислоты, содержащие слабосвязанную серу), реакция Миллона (на тирозин), реакция Сакагучи (на аргинин) и др.
При проведении цветных реакций на белки и аминокислоты необходимо предварительно составить следующую таблицу:
Цветные реакции на белки (качественные реакции)
| № | Название реакции | Применяемые реактивы | Появление окрашивания |
Что открывает данная реакция |
| 1 | Биуретовая и т.д. | |||
| Выводы … |
Биуретовая реакция – качественная на все без исключения белки, а также продукты их неполного гидролиза, которые содержат не менее двух пептидных связей.
Принцип метода. Биуретовая реакция обусловлена присутствием в белках пептидных связей (- СО – NH -), которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные в красно-фиолетовый цвет медные солеобразные комплексы. Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH2-CO-NH-CO-NH2), оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин, треонин, аспарагин).
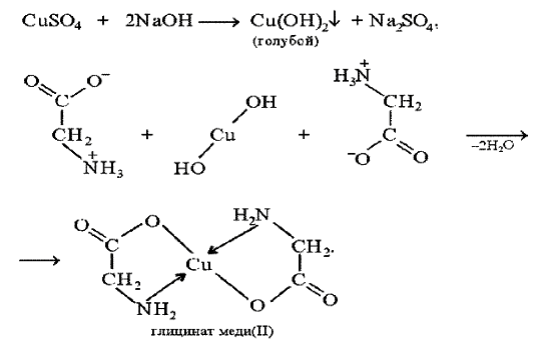
Биуретовая реакция с глицином
Порядок выполнения работы.
К 1 мл исследуемого 1% раствора белка добавляют равный объем 10 % раствора гидроксида натрия (NaOH) щелочи и затем 2-3 капли 1 % раствора сульфата меди (CuSO4). разбавленного, почти бесцветного раствора медного купороса.
При положительной реакции появляется фиолетовая окраска с красным либо синим оттенком.
Вывод:
Принцип метода. Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Порядок выполнения работы.
В пробирку наливают 1 мл неразбавленного куриного белка, прибавляют 2 мл 20%-го раствора гидроксида натрия. Смесь осторожно кипятят (чтобы смесь не выбросило).
При этом выделяется аммиак, который обнаруживается по посинению влажной лакмусовой бумажки, поднесенной к отверстию пробирки (не касаться стенки). Образующийся незначительный осадок растворяется при кипении, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Химизм реакции:
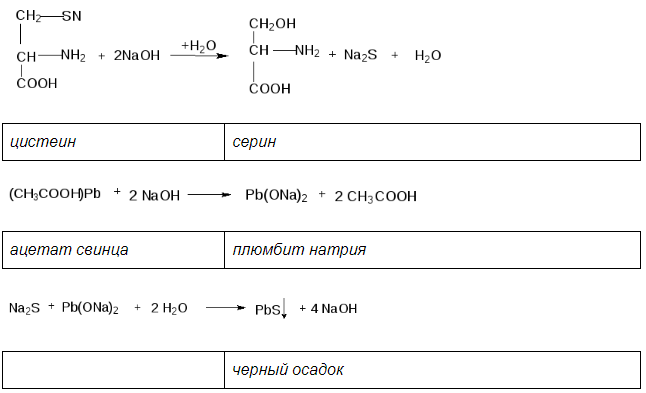
В пробирку наливают 1 мл. неразбавленного куриного белка добавляют 2 мл. концентрированного раствора щелочи, кладут несколько кипятильников. К горячему раствору добавляют раствор плюмбита натрия – образуется желто-бурое или черное окрашивание. (Плюмбит натрия готовят следующим образом: к 1 мл уксуснокислого свинца добавляют раствор щелочи по каплям до растворения образующего вначале осадка гидроксида свинца).
При наличии в молекуле белка серосодержащих аминокислот (цистина, цистеина) из этих аминокислот постепенно отщепляется сера в виде иона в степени окисления – 2, наличие которого и обнаруживается ионом свинца, образующим с ионом серы черный нерастворимый сульфид свинца:
Принцип метода. Эта реакция используется для обнаружения a-аминокислот, содержащих ароматические радикалы. Тирозин, триптофан, фенилаланин при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные, имеющие желтую окраску. В щелочной среде нитропроизводные этих a-аминокислот дают соли, окрашенные в оранжевый цвет. Желатин, например, не содержащий ароматических аминокислот, не дает ксантопротеиновой пробы.
Порядок выполнения работы.
К 1 мл 10 %-го раствора белка куриного яйца добавляют 0,5 мл концентрированной азотной кислоты. В результате коагуляции белка в содержимом пробирки образуется белый осадок или помутнение. При нагревании раствор и осадок окрашиваются в ярко-желтый цвет. При этом осадок почти полностью растворяется в результате гидролиза. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия (до появления оранжевой окраски раствора).
Рассмотрим механизм ксантопротеиновой реакции по радикалу тирозина:
Оформление опыта: сделать вывод и написать уравнение реакции.
Принцип метода. Белки, содержащие триптофан, в присутствии глиоксиловой и серной кислот дают красно-фиолетовое окрашивание. Реакция основана на способности триптофана взаимодействовать в кислой среде с альдегидами глиоксиловой кислоты (являющейся примесью к концентрированной уксусной кислоте) с образованием окрашенных продуктов конденсации. Реакция протекает по уравнению:.png)
Желатин не дает этой реакции, т.к. он не содержит триптофана. Окраска возникает за счет реакции триптофана с глиоксиловой кислотой, всегда присутствующей в уксусной кислоте в виде примеси.
Эту же реакцию на триптофан можно провести, используя вместо уксусной кислоты формальдегид 2,5%-ный раствор концентрированной H2SO4. Раствор перемешать и через 2-3 мин. добавить при взбалтывании 10 капель 5%-ного нитрита натрия. Развивается интенсивно-фиолетовое окрашивание, на этом основан принцип метода реакции.
Порядок выполнения работы.
В пробирку наливают несколько капель неразбавленного белка и прибавляют 2 мл. ледяной уксусной кислоты и несколько капель глиоксиловой кислоты. Смесь слегка нагревают до растворения образующегося осадка, охлаждают и, сильно наклонив пробирку, осторожно по стенке приливают концентрированную H2SO4 так, чтобы обе жидкости не смешивались.
Через 5-10 минут на границе раздела двух слоев наблюдают образование красно-фиолетового кольца.
Оформление опыта: сделать вывод и написать уравнение реакции.
Принцип метода. a-Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты. Реакция идет по схеме:
Реакция с нингидрином используется для визуального обнаружения a-аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Продукт этой реакции содержит в своем составе радикал (R) исходной аминокислоты, который обусловливает различную окраску: голубую, красную, и т.д. соединений, возникающих при реакции аминокислот с нингидрином.
В настоящее время нингидриновая реакция широко используется как для открытия отдельных аминокислот, так и для определения их количества.
Порядок выполнения работы.
В пробирку наливают 1 мл 1-10%-го разбавленного раствора белка куриного яйца и 1-2 мл 1%-го раствора нингидрина в ацетоне. Содержимое пробирки перемешивают и в течение 2-3 мин осторожно нагревают на водяной бане до появления сине-фиолетового окрашивания, свидетельствующее о присутствии в белке α-аминокислот.
Оформление опыта: сделать вывод и написать уравнение реакции.
Принцип метода. Эта реакция на аминокислоту аргинин основана на взаимодействии аргинина с a-нафтолом в присутствии окислителя. Ее механизм еще полностью не выяснен. По-видимому, реакция осуществляется по следующему уравнению:
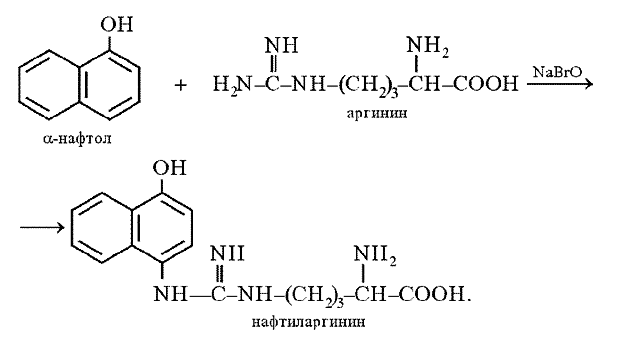
Поскольку производные хинониминов (в данном случае нафтохинона), у которых водород иминогруппы –NH– замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления оставшихся NH-групп аргининового остатка и бензольного ядра a-нафтола:
Порядок выполнения работы.
К 2 мл. 1%-го разбавленного раствора белка куриного яйца добавляют 2 мл. 10%-го гидроксида натрия (NaOH) и несколько капель 0,2%-ного спиртового раствора α-нафтола. Содержимое пробирки хорошо перемешивают. Затем приливают 0,5 мл. гипобромита натрия (NaBrO) или гипохлорита натрия (натрий хлорноватистокислый – NaOCl), перемешивают. Тотчас появляется красное, постепенно усиливающееся окрашивание.
Немедленно добавляют 1 мл 40%-го раствора мочевины для стабилизации, быстро развивающегося оранжево-красного окрашивания.
Эта реакция характерна для соединений, содержащих остаток гуанидина
N H = C –NH2,
H = C –NH2,
NH2
и указывает на присутствие в белковой молекуле аминокислоты-аргинина:
NH = C –NH – (CH2)3 –CH –COOH
NH2 NH2
Оформление опыта: сделать вывод и написать уравнение реакции.





В данной статье речь пойдет о профессиях будущего, которые только набирают обороты в современное время и по прогнозам продвинутся далеко вперед в будущем. Какими навыками должен обладать человек, чтобы освоить такую специальность, и к каким советам лучше прислушаться.

Искусственный интеллект и автоматизация промышленности повлияли на появление новых профессий. Именно они должны стать специальностями будущего, которые требуют от человека отдельной подготовки и получения навыков. В условиях меняющегося рынка приходится адаптироваться к новым условиям. В предложенной статье мы разберем профессии будущего, способные стать востребованными уже в ближайшее время.
В юношеском возрасте крайне сложно определиться с конкретной профессией. В условиях меняющегося мира сделать это еще сложнее. Подростку трудно представить, что его родители смогли продержаться на одном рабочем месте на протяжении всей жизни. Современные реалии заставляют нас получать новые навыки, посещать различные курсы и кардинально менять профессию.
Но всегда нужно оставаться верным мысли о том, чтобы выбирать специальность, исходя из собственных интересов. Только в этом случае вы добьетесь успеха в собственном деле и получите удовлетворение от проделанной работы.
Новые технологии не смогут окончательно вытеснить из профессий присутствие человека. К направлениям, которые не потеряют своей актуальности, относятся:
С внедрением на рынке труда искусственного интеллекта, автоматизации и робототехники, предполагается снижение потребности в физических и базовых когнитивных навыках. А на технологические и социально-эмоциональные навыки спрос возрастает. От работников будущего требуются в первую очередь следующие способности:
Фото: https://www.piqsels.com
Выбирая профессию, необходимо ориентироваться на предпочтения в различных областях наук, которые подразделяются следующим образом:
Данная классификация наук помогает сначала выбрать направление в обучении, а затем и профессию.
Профессиям будущего не обучают в университетах, учебные заведения не успевают адаптироваться к ним. Подбор обучающей программы, учебных материалов, поиск преподавателей занимает слишком много времени. Поэтому нужно брать инициативу в собственные руки и начинать изучение новых профессий.
Эксперты на рынке труда советуют обратить внимание на специальности, стремительно набирающие популярность:
Фото: https://www.piqsels.com
Эксперты также считают, что ныне существующие профессии не утратят своей актуальность и в будущем. Такими же востребованными специальностями станут следующие:
Выбирая профессию, нужно ориентироваться на личностные факторы:
Фото: https://www.piqsels.com
Если выбор профессии стоит перед выпускником школы, нужно следовать таким советам:
Эти навыки важны при выборе современных профессий, так как гибкость и адаптивность позволяют быстро подстраиваться под происходящие в мире изменения.
Не всегда изначальный выбор специальности совпадает с дальнейшими предпочтениями человека. Ошибиться может каждый. В этом случае помогут именно адаптивность и гибкость, чтобы вовремя сориентироваться на профессиональном рынке. Человеку будет легче искать новые возможности и справляться с трудностями. Ошибки же не будут разочаровывать, а послужат стимулом к их исправлению и профессиональному росту.
Все мы разные и универсальных профессий не существует. Выбирать направление нужно исходя из индивидуальных качеств, собственных интересов и предпочтений.


Алгоритм для подсчёта числа дыхательных движений (чдд) и правила заполнение медицинской документации, заполнение температурного листа.

Цель:определить основные характеристики дыхания.
Показания:заболевания органов дыхания, и сердечно – сосудистой системы.
Противопоказания:нет.
Оснащение:часы (секундомер), температурный лист или лист сестринского наблюдения, ручка бумага.
Алгоритм:
| Этапы | Обоснование |
| I. Подготовка к процедуре:1. Доброжелательно и уважительно представиться пациенту. Уточнить, как к нему обращаться. | Установление контакта с пациентом. |
| 2. Предупредить пациента, что будет проведено исследование пульса. | Исключается возможность управления дыханием. |
| 3. Получить согласие пациента на проведение процедуры. | Обеспечиваются права пациента на информацию. |
| 4. Вымыть и осушить руки. | Обеспечение инфекционной безопасности |
| 5. Попросить пациента или помочь ему удобно лечь (сесть) в постели, чтобы видеть верхнюю часть его грудной клетки и живота (эпигастральную область). | Для уточнения (определения) типа и ритма дыхания. |
| 6. Определить тип и ритм дыхания. | Обеспечивается точность (достоверность) подсчета ЧДД. |
| II. Выполнение процедуры:7. Взять пациента за руку так, как для исследования пульса, наблюдать за экскурсией грудной клетки или за движениями эпигастральной области живота пациента. Считать дыхательные движения за 1 минуту. Примечание: если не удается наблюдать экскурсию грудной клетки, то положить руки (пациента и свою) на грудную клетку (у женщин) или на эпигастральную область (у мужчин), имитируя исследование пульса (продолжая держать руку за запястье) | Определение ЧДД |
| 8. Зафиксировать результат на бумаге и перенести данные в лист сестринского наблюдения или температурный лист. | Обеспечение контроля за состоянием органов дыхания и сердечно-сосудистой системы. |
| III. Окончание процедуры:9. Вымыть и осушить руки. | Обеспечение инфекционной безопасности. |
Цель:правила заполнение медицинской документации.
Показания:регистрация результатов обследования пациента.
Противопоказания:нет.
Оснащение:температурный лист, ручки (или карандаши) с красной, синей пастой.
Алгоритм:
| Этапы | Обоснование |
| I. Подготовка к манипуляции. 1. Приготовить стандартный температурный лист. 2. Приготовить синий или черный карандаш (или пасту), красный карандаш (или пасту). II. Выполнение манипуляции. 3. Утреннюю температуру отметить точкой в графе «У», вечернюю – в графе «В». 4. Отметить верхнюю границу (систолического) и нижнюю границу (диастолического) артериального давления красным карандашом (или пастой). 5. В графе «У» отметить точкой результаты подсчета пульса утром, а в графе «В» результаты подсчета пульса вечером. 6. В графе «Дыхание» записать подсчет числа дыхательных движений в 1 мин.. 7. В графе «Вес» сделать отметку о данных массы тела пациента. 8. В графе «Выпито жидкости» отметить количество жидкости, поступившей в организм пациента. 9. В графе «Суточное количество мочи» отметить количество мочи, выделенное пациентом за сутки. 10. В графе «Стул» отметить знаком + данные о дефекации. 11. В графе «Ванна» отметить знаком + о проведении санитарной обработки пациенту. III. Окончание манипуляции. 4. Соединить точки утренней и вечерней температуры. 5. Соединить точки результатов подсчета пульса. 6. Красным карандашом обозначить в виде столбика АД. |
Правила заполнения медицинской документации. Эффективное прочтение результатов обследования пациента. Достоверность результата. Достоверность результата. Достоверность результата. Информация для лечащего врача. Обеспечение преемственности в сестринском уходе. Информация для лечащего врача. Обеспечение преемственности в сестринском уходе. Информация для лечащего врача. Обеспечение преемственности в сестринском уходе. Информация для лечащего врача. Обеспечение преемственности в сестринском уходе. Получение температурной кривой. Графическое отображение результатов пульса. Эффективность заполнения медицинской документации. |

